SAMENVATTING VAN DE PRODUCTKENMERKEN
1. NAAM VAN HET GENEESMIDDEL
Dupixent 300 mg oplossing voor injectie in een voorgevulde spuit
Dupixent 300 mg oplossing voor injectie in een voorgevulde pen
2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING
Dupilumab 300 mg oplossing voor injectie in een voorgevulde spuit
Elke voorgevulde spuit voor eenmalig gebruik bevat 300 mg dupilumab in een oplossing van 2 ml (150 mg/ml).
Dupilumab 300 mg oplossing voor injectie in een voorgevulde pen
Elke voorgevulde pen voor eenmalig gebruik bevat 300 mg dupilumab in een oplossing van 2 ml (150 mg/ml).
Dupilumab is een volledig humaan monoklonaal antilichaam en wordt geproduceerd uit ovariumcellen van de Chinese hamster (CHO, Chinese hamster ovary) door middel van recombinant-DNA-technologie.
Hulpstoffen met bekend effect
Dit geneesmiddel bevat 4 mg polysorbaat 80 in elke dosis van 300 mg (2 ml). Polysorbaten kunnen allergische reacties veroorzaken.
Voor de volledige lijst van hulpstoffen, zie rubriek 6.1.
3. FARMACEUTISCHE VORM
Oplossing voor injectie (injectie)
Een heldere tot licht doorschijnende, kleurloze tot lichtgele steriele oplossing, die vrij is van zichtbare deeltjes, met een pH van ongeveer 5,9.
4. KLINISCHE GEGEVENS
4.1 Therapeutische indicaties
Atopische dermatitis
Volwassenen en adolescenten
Dupixent is geïndiceerd voor de behandeling van matige tot ernstige atopische dermatitis bij volwassenen en adolescenten in de leeftijd van 12 jaar en ouder die in aanmerking komen voor een systemische behandeling.
Kinderen van 6 maanden tot en met 11 jaar
Dupixent is geïndiceerd voor de behandeling van ernstige atopische dermatitis bij kinderen van 6 maanden tot en met 11 jaar oud die in aanmerking komen voor systemische behandeling.
Astma
Volwassenen en adolescenten
Dupixent is geïndiceerd voor gebruik bij volwassenen en adolescenten van 12 jaar en ouder als aanvullende onderhoudsbehandeling van ernstig astma met type 2 inflammatie gekenmerkt door verhoogde bloedeosinofielen en/of verhoogde fractie van stikstofmonoxide in de uitgeademde lucht (FeNO), zie rubriek 5.1, die onvoldoende kunnen worden behandeld met hooggedoseerde geïnhaleerde corticosteroïden (ICS) plus een ander geneesmiddel voor onderhoudsbehandeling.
Kinderen van 6 tot en met 11 jaar
Dupixent is geïndiceerd voor gebruik bij kinderen van 6 tot en met 11 jaar oud als aanvullende onderhoudsbehandeling van ernstig astma met type 2 inflammatie gekenmerkt door verhoogde bloedeosinofielen en/of verhoogde fractie van stikstofmonoxide in de uitgeademde lucht (FeNO), zie rubriek 5.1, die onvoldoende kunnen worden behandeld met gemiddeld tot hooggedoseerde geïnhaleerde corticosteroïden (ICS) plus een ander geneesmiddel voor onderhoudsbehandeling.
Chronische rinosinusitis met neuspoliepen (CRSwNP)
Dupixent is geïndiceerd als aanvullende therapie met intranasale corticosteroïden voor de behandeling van volwassenen met ernstige CRSwNP voor wie behandeling met systemische corticosteroïden en/of chirurgie geen adequate ziektecontrole biedt.
Prurigo Nodularis (PN)
Dupixent is geïndiceerd bij de behandeling van volwassenen met matige tot ernstige prurigo nodularis (PN) die in aanmerking komen voor systemische therapie.
Eosinofiele oesofagitis (EoE)
Dupixent is geïndiceerd voor de behandeling van eosinofiele oesofagitis bij volwassenen, adolescenten en kinderen van 1 jaar en ouder, met een gewicht van ten minste 15 kg, die onvoldoende onder controle zijn met, intolerant of geen kandidaat zijn voor een conventionele behandeling met geneesmiddelen (zie rubriek 5.1).
Chronische obstructieve longziekte (COPD)
Dupixent is geïndiceerd bij volwassenen als aanvullende onderhoudsbehandeling voor ongecontroleerde chronische obstructieve longziekte (COPD) gekenmerkt door verhoogde bloedeosinofielen op een combinatie van een geïnhaleerd corticosteroïd (ICS), een langwerkende bèta2-agonist (LABA) en een langwerkende muscarine-antagonist (LAMA), of op een combinatie van een LABA en een LAMA als ICS niet aangewezen is (zie rubriek 5.1).
4.2 Dosering en wijze van toediening
De behandeling dient te worden opgestart door beroepsbeoefenaren in de gezondheidszorg die bekend zijn met de diagnose en behandeling van de aandoeningen waarvoor dupilumab is geïndiceerd (zie rubriek 4.1).
Dosering
Atopische dermatitis
Volwassenen
De aanbevolen dosis dupilumab voor volwassen patiënten is een startdosis van 600 mg (twee injecties van 300 mg), gevolgd door 300 mg eenmaal per twee weken, toegediend als subcutane injectie.
Adolescenten (12 tot en met 17 jaar oud)
De aanbevolen dosis dupilumab voor adolescente patiënten van 12 tot en met 17 jaar is gespecificeerd in tabel 1.
Tabel 1: Dosis dupilumab voor subcutane toediening bij adolescente patiënten van 12 tot en met 17 jaar oud met atopische dermatitis
Lichaamsgewicht van de patiënt | Initiële dosis | Volgende doses |
minder dan 60 kg | 400 mg (twee injecties van 200 mg) | 200 mg |
60 kg of meer | 600 mg (twee injecties van 300 mg) | 300 mg |
Kinderen van 6 tot en met 11 jaar oud
De aanbevolen dosis dupilumab voor kinderen van 6 tot en met 11 jaar oud is gespecificeerd in tabel 2.
Tabel 2: Dosis dupilumab voor subcutane toediening bij kinderen van 6 tot en met 11 jaar oud met atopische dermatitis
Lichaamsgewicht van de patiënt | Initiële dosis | Volgende doses |
15 kg tot | 300 mg (één injectie van 300 mg) op dag 1, gevolgd door 300 mg op dag 15 | 300 mg om de vier weken (Q4W)*, |
60 kg of meer | 600 mg (twee injecties van 300 mg) | 300 mg om de twee weken (Q2W) |
* de dosis kan naargelang het oordeel van de arts verhoogd worden naar 200 mg Q2W bij patiënten met een lichaamsgewicht van 15 kg tot minder dan 60 kg.
Kinderen van 6 maanden tot en met 5 jaar
De aanbevolen dosis dupilumab voor kinderen van 6 maanden tot en met 5 jaar oud is gespecificeerd in tabel 3.
Tabel 3: Dosis dupilumab voor subcutane toediening bij kinderen van 6 maanden tot en met 5 jaar oud met atopische dermatitis | ||
Lichaamsgewicht van de patiënt | Initiële dosis | Volgende doses |
5 kg tot minder dan 15 kg | 200 mg (één injectie van 200 mg) | 200 mg om de vier weken (Q4W) |
15 kg tot minder dan 30 kg | 300 mg (één injectie van 300 mg) | 300 mg om de vier weken (Q4W) |
Dupilumab kan gebruikt worden met of zonder behandeling met topische corticosteroïden. Het is mogelijk topische calcineurineremmers te gebruiken, maar dit zou moeten worden beperkt tot enkel de probleemgebieden, zoals het gezicht, de hals, intertrigineuze gebieden en de genitaliën.
Als patiënten na 16 weken behandeling voor atopische dermatitis geen reactie vertonen, overweeg dan de behandeling te stoppen. Sommige patiënten met een initiële gedeeltelijke respons kunnen daarna verbetering ervaren met voortzetting van de behandeling na 16 weken. Als een onderbreking van de behandeling met dupilumab noodzakelijk wordt, kunnen patiënten nog steeds met succes opnieuw behandeld worden.
Astma
Volwassenen en adolescenten
De aanbevolen dosering dupilumab voor volwassenen en adolescenten (van 12 jaar en ouder) is:
- Voor patiënten met ernstig astma en die orale corticosteroïden gebruiken, of voor patiënten met ernstig astma en comorbide matige tot ernstige atopische dermatitis of volwassenen met comorbide ernstige chronische rinosinusitis met neuspoliepen, een initiële dosis van 600 mg (twee injecties van 300 mg), gevolgd door 300 mg eenmaal per twee weken, toegediend als subcutane injectie.
- Voor alle andere patiënten een initiële dosis van 400 mg (twee injecties van 200 mg), gevolgd door 200 mg eenmaal per twee weken, toegediend als subcutane injectie.
Kinderen van 6 tot en met 11 jaar
De aanbevolen dosis dupilumab voor pediatrische patiënten van 6 tot en met 11 jaar staat vermeld in tabel 4.
Tabel 4: Dosis dupilumab voor subcutane toediening bij kinderen van 6 tot en met 11 jaar met astma | |
Lichaamsgewicht | Eerste en daaropvolgende doses |
15 tot minder dan 30 kg | 300 mg om de vier weken (Q4W) |
30 tot minder dan 60 kg | 200 mg om de twee weken (Q2W) |
60 kg of meer | 200 mg om de twee weken (Q2W) |
Voor pediatrische patiënten (6 tot en met 11 jaar) met astma en comorbide ernstige atopische dermatitis moet volgens de goedgekeurde indicatie de aanbevolen dosis in tabel 2 worden gevolgd.
Patiënten die gelijktijdig orale corticosteroïden ontvangen, kunnen hun dosis steroïden verlagen als er klinische verbetering is opgetreden met dupilumab (zie rubriek 5.1). Het verlagen van steroïden dient geleidelijk te gebeuren (zie rubriek 4.4).
Dupilumab is bedoeld voor langdurige behandeling. De noodzaak van het voortzetten van de behandeling dient ten minste jaarlijks geëvalueerd te worden op basis van de beoordeling van de arts op de mate van astmacontrole van de patiënt.
Chronische rinosinusitis met neuspoliepen (CRSwNP)
De aanbevolen dosis dupilumab voor volwassen patiënten is een initiële dosis van 300 mg, gevolgd door 300 mg eenmaal per twee weken.
Dupilumab is bedoeld voor langdurige behandeling. Als patiënten na 24 weken behandeling voor CRSwNP geen reactie vertonen, overweeg dan de behandeling te stoppen. Sommige patiënten met een initiële gedeeltelijke respons kunnen daarna verbetering ervaren met voortzetting van de behandeling na 24 weken.
Prurigo Nodularis (PN)
De aanbevolen dosis dupilumab voor volwassen patiënten is een initiële dosis van 600 mg (twee injecties van 300 mg), gevolgd door 300 mg eenmaal per twee weken.
Dupilumab kan worden gebruikt met of zonder topische corticosteroïden.
Er zijn klinische onderzoeksgegevens beschikbaar over patiënten met PN die maximaal 24 weken zijn behandeld. Als patiënten na 24 weken behandeling voor PN geen reactie vertonen, overweeg dan de behandeling te stoppen.
Eosinofiele oesofagitis (EoE)
De aanbevolen dosis dupilumab voor volwassenen, adolescenten en kinderen van 1 jaar en ouder, met een gewicht van ten minste 15 kg, wordt gespecificeerd in tabel 5.
Tabel 5: Dosis dupilumab voor subcutane toediening bij volwassenen, adolescenten en kinderen van 1 jaar en ouder met EoE
Lichaamsgewicht van de patiënt | Dosis |
15 kg tot minder dan 30 kg | 200 mg om de twee weken (Q2W) |
30 kg tot minder dan 40 kg | 300 mg om de twee weken (Q2W) |
40 kg of meer | 300 mg elke week (QW) |
Dupilumab is bedoeld voor langdurige behandeling.
Chronische obstructieve longziekte (COPD)
De aanbevolen dosis dupilumab voor volwassen patiënten is 300 mg om de twee weken.
Dupilumab is bedoeld voor langdurige behandeling. Dosering langer dan 52 weken is niet onderzocht. Er moet worden overwogen om de behandeling stop te zetten bij patiënten die geen respons vertonen na 52 weken behandeling van COPD.
Gemiste dosis
In het geval dat een wekelijkse dosis wordt gemist, dien de dosis dan zo snel mogelijk toe, waarbij een nieuw schema wordt gestart op basis van deze datum.
Als een tweewekelijkse dosis wordt gemist, dien de injectie dan toe binnen 7 dagen na de gemiste dosis en hervat het oorspronkelijke schema van de patiënt. Als de gemiste dosis niet binnen 7 dagen wordt toegediend, wacht dan tot de volgende dosis volgens het oorspronkelijke schema.
Als een vierwekelijkse dosis wordt gemist, dien de injectie dan toe binnen 7 dagen na de gemiste dosis en hervat het oorspronkelijke schema van de patiënt. Als de gemiste dosis niet binnen 7 dagen wordt toegediend, dien de dosis toe en begin met een nieuw schema op basis van deze datum.
Speciale populaties
Ouderen
Voor ouderen (≥ 65 jaar) hoeft de dosis niet te worden aangepast (zie rubriek 5.2).
Nierfunctiestoornis
Er is geen dosisaanpassing nodig bij patiënten met een lichte of matige nierfunctiestoornis. Er is zeer beperkte informatie beschikbaar over patiënten met een ernstige nierfunctiestoornis (zie rubriek 5.2).
Leverfunctiestoornis
Er is geen informatie beschikbaar over patiënten met een leverfunctiestoornis (zie rubriek 5.2).
Lichaamsgewicht
De dosis hoeft niet te worden aangepast aan het lichaamsgewicht voor patiënten met astma en EoE van 12 jaar en ouder of bij volwassenen met atopische dermatitis, CRSwNP, PN of COPD (zie rubriek 5.2).
Pediatrische patiënten
De veiligheid en werkzaamheid van dupilumab bij kinderen met atopische dermatitis jonger dan 6 maanden oud zijn niet vastgesteld. De veiligheid en werkzaamheid van dupilumab bij kinderen met een lichaamsgewicht van < 5 kg zijn niet vastgesteld. Er zijn geen gegevens beschikbaar.
De veiligheid en werkzaamheid van dupilumab bij kinderen met ernstig astma jonger dan 6 jaar zijn niet vastgesteld. Er zijn geen gegevens beschikbaar.
De veiligheid en werkzaamheid bij kinderen met CRSwNP jonger dan 18 jaar zijn niet vastgesteld. Er zijn geen gegevens beschikbaar.
De veiligheid en werkzaamheid van dupilumab bij kinderen met PN jonger dan 18 jaar zijn niet vastgesteld. Er zijn geen gegevens beschikbaar.
De veiligheid en werkzaamheid van dupilumab bij kinderen met EoE jonger dan 1 jaar, of met een lichaamsgewicht <15 kg, zijn niet vastgesteld.
De veiligheid en werkzaamheid van dupilumab bij kinderen met COPD jonger dan 18 jaar zijn niet vastgesteld. Er zijn geen gegevens beschikbaar.
Wijze van toediening
Subcutaan gebruik
De voorgevulde pen met dupilumab is bestemd voor gebruik bij volwassen en pediatrische patiënten van 2 jaar en ouder.
De voorgevulde spuit met dupilumab is bestemd voor gebruik bij volwassen en pediatrische patiënten van 6 maanden en ouder. De voorgevulde pen met dupilumab is niet bedoeld voor gebruik bij kinderen jonger dan 2 jaar.
Dupilumab wordt toegediend door middel van subcutane injectie in de dij of buik, met uitzondering van het gebied van 5 cm rond de navel. Indien iemand anders de injectie toedient, kan de bovenarm ook worden gebruikt.
Elke voorgevulde spuit of voorgevulde pen dient enkel voor eenmalig gebruik.
Voor indicaties die een initiële dosis van 600 mg vereisen (zie Dosering in rubriek 4.2), moeten twee injecties van 300 mg opeenvolgend worden toegediend op verschillende injectieplaatsen.
Het wordt aanbevolen om van injectieplaats te wisselen bij iedere injectie. Dupilumab niet injecteren in pijnlijke, beschadigde of gekneusde huid of in de buurt van littekenweefsel.
Een patiënt mag zelf dupilumab toedienen of de mantelzorger van de patiënt kan dupilumab toedienen indien de beroepsbeoefenaar in de gezondheidszorg bepaalt dat dit aangewezen is. De patiënt en/of mantelzorgers moeten goed worden geïnstrueerd in het voorbereiden en toedienen van dupilumab voorafgaand aan het gebruik, volgens de rubriek “Instructies voor gebruik” aan het einde van de bijsluiter. Bij kinderen van 12 jaar en ouder wordt aanbevolen dupilumab toe te laten dienen door of onder toezicht van een volwassene. Bij kinderen van 6 maanden tot jonger dan 12 jaar dient dupilumab te worden toegediend door een verzorger.
4.3 Contra-indicaties
Overgevoeligheid voor de werkzame stof(fen) of voor een van de in rubriek 6.1 vermelde hulpstof(fen).
4.8 Bijwerkingen
Samenvatting van het veiligheidsprofiel
De meest voorkomende bijwerkingen bij atopische dermatitis, astma en CRSwNP zijn reacties op de injectieplaats (waaronder erytheem, oedeem, pruritus, pijn en zwelling), conjunctivitis, allergische conjunctivitis, artralgie, orale herpes en eosinofilie. Een bijkomende ongewenste reactie van injectieplaatskneuzing werd gemeld bij EoE en COPD. Bijkomende bijwerkingen met name verharding op de injectieplaats, huiduitslag op de injectieplaats en dermatitis op de injectieplaats werden gemeld bij COPD. Er werden zeldzame gevallen van serumziekte/serumziekteachtige reactie, anafylactische reactie en ulceratieve keratitis gemeld (zie rubriek 4.4).
Tabel met bijwerkingen
De veiligheidsgegevens van dupilumab die in tabel 6 worden weergegeven, zijn hoofdzakelijk afkomstig van 12 gerandomiseerde placebogecontroleerde onderzoeken, met onder meer patiënten met atopische dermatitis, astma en CRSwNP. Deze onderzoeken, waarin 4.206 patiënten dupilumab en 2.326 patiënten een placebo kregen in de gecontroleerde periode, zijn representatief voor het algemene veiligheidsprofiel van dupilumab.
In tabel 6 worden de bijwerkingen opgesomd die in klinische onderzoeken en/of in de postmarketingsetting zijn waargenomen, gepresenteerd per systeem/orgaanklasse en frequentie, volgens de volgende categorieën: zeer vaak (≥ 1/10); vaak (≥ 1/100, < 1/10); soms (≥ 1/1.000, < 1/100); zelden (≥ 1/10.000, < 1/1.000); zeer zelden (< 1/10.000); niet bekend (kan met de beschikbare gegevens niet worden bepaald). Binnen elke frequentiegroep worden de bijwerkingen weergegeven in volgorde van afnemende ernst.
Tabel 6: Lijst van bijwerkingen
Systeem/orgaanklasse volgens MedDRA | Frequentie | Bijwerking |
Infecties en parasitaire aandoeningen | Vaak | Conjunctivitis* |
Bloed- en lymfestelselaandoeningen | Vaak | Eosinofilie |
Immuunsysteemaandoeningen | Soms | Angio-oedeem# |
Oogaandoeningen | Vaak | Allergische conjunctivitis* |
Huid- en onderhuidaan-doeningen | Soms | Rash in gezicht# |
Skeletspierstelsel- en bindweefselaandoeningen | Vaak | Artralgie# |
Algemene aandoeningen en toedieningsplaatsstoornissen | Vaak | Reacties op de injectieplaats (waaronder erytheem, oedeem, pruritus, pijn, zwelling en blauwe plekken) |
* oogaandoeningen en orale herpes deden zich vooral voor in onderzoeken naar atopische dermatitis.
† de frequenties voor oculaire pruritus, blefaritis en droog oog waren vaak en ulceratieve keratitis deed zich soms voor in onderzoeken naar atopische dermatitis.
#uit postmarketing rapportering
Beschrijving van geselecteerde bijwerkingen
Overgevoeligheid
Er zijn na toediening van dupilumab gevallen van een anafylactische reactie, angio-oedeem, serumziekte of een serumziekteachtige reactie gemeld (zie rubriek 4.4).
Conjunctivitis en keratitis gerelateerde voorvallen
Conjunctivitis en keratitis kwamen vaker voor bij patiënten met atopische dermatitis die dupilumab ontvingen ten opzichte van placebo in onderzoeken naar atopische dermatitis. De meeste patiënten met conjunctivitis of keratitis herstelden of waren herstellende tijdens de behandelingsperiode. In het langetermijn OLE-onderzoek naar atopische dermatitis (AD-1225) bleven de respectieve percentages voor conjunctivitis en keratitis na 5 jaar vergelijkbaar met die van de dupilumab-groep in de placebogecontroleerde onderzoeken naar atopische dermatitis. Bij de patiënten met astma en COPD was de frequentie van conjunctivitis en keratitis laag en vergelijkbaar tussen dupilumab en placebo. Bij patiënten met CRSwNP of PN was de frequentie van conjunctivitis hoger met dupilumab dan met placebo, hoewel lager dan waargenomen bij patiënten met atopische dermatitis. Er werden geen gevallen van keratitis gemeld in de CRSwNP- of PN-ontwikkelingsprogramma’s. Bij de patiënten met EoE was de frequentie van conjunctivitis laag en vergelijkbaar tussen de dupilumab- en de placebogroep. Er waren geen gevallen van keratitis in het EoE-ontwikkelingsprogramma (zie rubriek 4.4).
Eczema herpeticum
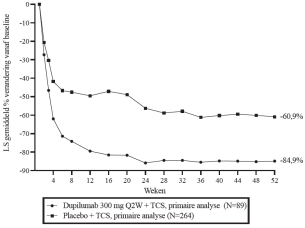
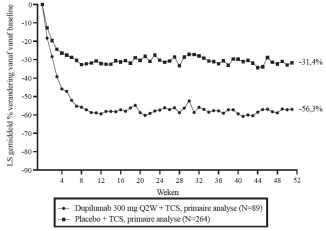
Eczema herpeticum werd gemeld bij < 1% van de dupilumab groepen en bij < 1% van de placebogroep in de 16 weken durende monotherapie onderzoeken bij volwassenen met atopische dermatitis. In het 52 weken durende dupilumab + TCS (Topical corticosteroids) onderzoek bij volwassenen met atopische dermatitis is eczema herpeticum gemeld bij 0,2% van de dupilumab + TCS-groep en 1,9% van de placebo + TCS-groep. Deze percentages bleven stabiel na 5 jaar in het langetermijn OLE-onderzoek (AD-1225).
Eosinofilie
Patiënten die werden behandeld met dupilumab hadden een grotere gemiddelde initiële verhoging vanaf de baseline van het aantal eosinofielen in vergelijking met patiënten die met een placebo werden behandeld bij de indicaties atopische dermatitis, astma, CRSwNP en COPD. Het aantal eosinofielen nam af gedurende de onderzoeksbehandeling tot nabij het niveau bij baseline en daalde tot de baselinewaarden tijdens het astma open-label uitbreidingsonderzoek naar de veiligheid (TRAVERSE). Het gemiddeld aantal eosinofielen in het bloed daalde tot onder de baseline tegen Week 20 en bleef tot 5 jaar gehandhaafd in het langetermijn OLE-onderzoek (AD-1225). Ten opzichte van behandeling met placebo werd geen toename van het gemiddelde aantal eosinofielen waargenomen bij PN (PRIME en PRIME2). Tijdens de onderzoeksbehandeling bij EoE en COPD (BOREAS en NOTUS) nam het gemiddeld en mediaan aantal eosinofielen in het bloed af tot nabij het niveau bij baseline of het bleef onder het niveau bij baseline.
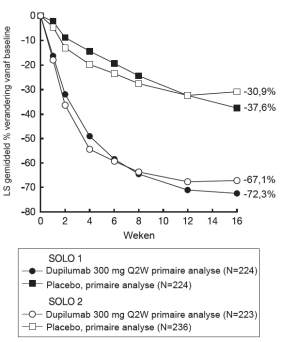
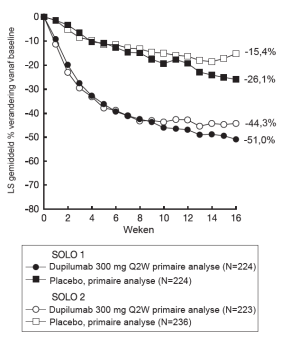
Tijdens de behandeling optredende eosinofilie (≥ 5.000 cellen/mcl) werd gemeld bij < 3% van de patiënten behandeld met dupilumab en < 0,5% bij patiënten die placebo ontvingen (onderzoeken SOLO1, SOLO2, AD-1021, DRI12544, QUEST en VOYAGE; SINUS-24 en SINUS-52; PRIME en PRIME2; TREET, deel A en B; BOREAS and NOTUS).
Tijdens de behandeling optredende eosinofilie (≥ 5.000 cellen/mcl) werd in onderzoek AD-1539 gemeld bij 8,4% van de met dupilumab behandelde patiënten en bij 0% van de met placebo behandelde patiënten, waarbij de mediane aantallen eosinofielen daalden tot onder de baselinewaarde aan het einde van de behandelingsperiode.
Infecties
In de 16 weken durende klinische monotherapie-onderzoeken bij volwassenen met atopische dermatitis werden ernstige infecties gemeld bij 1,0% van de patiënten die placebo kregen en bij 0,5% van de patiënten die werden behandeld met dupilumab. In het 52 weken durende CHRONOS-onderzoek bij volwassenen met atopische dermatitis werden ernstige infecties gemeld bij 0,6% van de patiënten die placebo kregen en bij 0,2% van de patiënten die werden behandeld met dupilumab. De percentages van ernstige infecties bleven stabiel na 5 jaar in het langetermijn OLE-onderzoek (AD-1225).
Er werd geen toename waargenomen in de totale incidentie van infecties met dupilumab in vergelijking met placebo in de veiligheidspool voor klinische onderzoeken naar astma. In de 24 weken durende veiligheidspool werden ernstige infecties gemeld bij 1,0% van de patiënten die werden behandeld met dupilumab en bij 1,1% van de patiënten die placebo kregen. In het 52 weken durende QUEST-onderzoek werden ernstige infecties gemeld bij 1,3% van de patiënten die werden behandeld met dupilumab en bij 1,4% van de patiënten die placebo kregen.
Er werd geen toename waargenomen in de totale incidentie van infecties met dupilumab in vergelijking met placebo in de veiligheidspool voor klinische onderzoeken naar CRSwNP. In het 52 weken durende SINUS-52-onderzoek werden ernstige infecties gemeld bij 1,3% van de patiënten die werden behandeld met dupilumab en bij 1,3% van de patiënten die placebo kregen.
Er werd geen toename waargenomen in de totale incidentie van infecties met dupilumab in vergelijking met placebo in de veiligheidspool voor klinische onderzoeken naar PN. In de veiligheidspool werden ernstige infecties gemeld bij 1,3% van de patiënten die werden behandeld met dupilumab en bij 1,3% van de patiënten die placebo kregen.
De totale incidentie van infecties was numeriek hoger bij dupilumab (32,0%) in vergelijking met placebo (24,8%) in de 24 weken durende veiligheidspool voor de EoE TREET-onderzoeken (deel A en B). De totale incidentie van infecties was numeriek hoger bij placebo (41,2%) in vergelijking met dupilumab (35,8%) in het EoE KIDS (deel A)-onderzoek. In de 24 weken durende veiligheidspool voor de EoE TREET-onderzoeken (deel A en B) zijn ernstige infecties gemeld bij 0,5% van de patiënten die behandeld werden met dupilumab en bij 0% van de patiënten behandeld met placebo. Er werden geen ernstige infecties gemeld in het EoE KIDS (deel A)-onderzoek. Infecties van de bovenste luchtwegen bestaande uit verschillende termen, waaronder, maar niet beperkt tot, COVID-19, sinusitis en infectie van de bovenste luchtwegen waren numeriek hoger met dupilumab (17,2%) in vergelijking met placebo (10,3%) in EoE TREET (deel A en B), en met dupilumab (26,9%) in vergelijking met placebo (20,6%) in het EoE KIDS (deel A)-onderzoek.
Er werd geen toename waargenomen in de algehele incidentie van infecties met dupilumab in vergelijking met placebo in de veiligheidspool voor klinische COPD-onderzoeken. Ernstige infecties werden gemeld bij 4,9% van de patiënten behandeld met dupilumab en 4,8% van de patiënten behandeld met placebo.
Immunogeniciteit
Zoals bij alle therapeutische eiwitten bestaat ook bij dupilumab kans op immunogeniciteit.
Reacties door antistoffen tegen het geneesmiddel (ADA’s) hadden over het algemeen geen invloed op de blootstelling aan, veiligheid of werkzaamheid van dupilumab.
Ongeveer 5% van de patiënten met atopische dermatitis, astma of CRSwNP die dupilumab 300 mg Q2W ontvingen gedurende 52 weken, ontwikkelden ADA's tegen dupilumab; ongeveer 2% vertoonde een blijvende ADA-respons, en ongeveer 2% had neutraliserende antistoffen. Er zijn gelijkaardige resultaten waargenomen bij volwassen patiënten met PN die dupilumab 300 mg Q2W gedurende 24 weken kregen, pediatrische patiënten (6 maanden tot en met 11 jaar oud) met atopische dermatitis die ofwel dupilumab 200 mg Q2W, 200 mg Q4W of 300 mg Q4W ontvingen gedurende 16 weken en patiënten (6 tot en met 11 jaar) met astma die dupilumab 100 mg Q2W of 200 mg Q2W kregen gedurende 52 weken.Vergelijkbare ADA‑responsen zijn waargenomen bij volwassen patiënten met atopische dermatitis die tot 5 jaar behandeld zijn met dupilumab in het langetermijn OLE-onderzoek (AD-1225).
Ongeveer 16% van de adolescente patiënten met atopische dermatitis die dupilumab 300 mg of 200 mg Q2W ontvingen gedurende 16 weken, ontwikkelden antistoffen tegen dupilumab; ongeveer 3% vertoonde een blijvende ADA-respons, en ongeveer 5% had neutraliserende antistoffen.
Ongeveer 9% van de patiënten met astma die dupilumab 200 mg Q2W ontvingen gedurende 52 weken, ontwikkelden antilichamen tegen dupilumab; ongeveer 4% vertoonde een blijvende ADA-respons, en ongeveer 4% had neutraliserende antistoffen.
Ongeveer 1% van de patiënten van 1 jaar en ouder met EoE die dupilumab 300 mg QW (≥40 kg), 300 mg Q2W (≥30 tot <60 kg), 200 mg Q2W (≥15 tot <30 kg) of 100 mg Q2W (≥5 tot <15 kg) gedurende 52 weken kregen toegediend, ontwikkelden antilichamen tegen dupilumab; de ADA-responsen waren niet aanhoudend noch neutraliserend.
Ongeveer 8% van de patiënten met COPD die 52 weken lang dupilumab 300 mg Q2W kregen, ontwikkelden antilichamen tegen dupilumab; ongeveer 3% vertoonde aanhoudende ADA-responsen en ongeveer 3% had neutraliserende antilichamen.
Ongeacht de leeftijd of de populatie was tot 7% van de patiënten in de placebogroepen positief voor antilichamen tegen dupilumab; tot 3% vertoonde een blijvende ADA-respons, en tot 2% had neutraliserende antistoffen.
Minder dan 1% van de patiënten die dupilumab ontvingen volgens het goedgekeurde toedieningsschema, vertoonde hoge titer ADA’s die gepaard ging met verminderde blootstelling en werkzaamheid. Daarnaast was er één patiënt met serumziekte en één met een serumziekteachtige reactie (< 0,1%) gepaard gaande met hoge ADA-titers (zie rubriek 4.4).
Pediatrische patiënten
Atopische dermatitis
Adolescenten (12 tot en met 17 jaar oud)
De veiligheid van dupilumab werd beoordeeld in een onderzoek met 250 patiënten van 12 tot en met 17 jaar oud met matige tot ernstige atopische dermatitis (AD-1526). Het veiligheidsprofiel van dupilumab bij deze patiënten die werden gevolgd tot en met Week 16 was vergelijkbaar met het veiligheidsprofiel uit onderzoeken bij volwassenen met atopische dermatitis.
Kinderen van 6 tot en met 11 jaar oud
De veiligheid van dupilumab werd beoordeeld in een onderzoek bij 367 patiënten van 6 tot en met 11 jaar oud met ernstige atopische dermatitis (AD-1652). Het veiligheidsprofiel van dupilumab met gelijktijdig TCS bij deze patiënten was tot en met week 16 vergelijkbaar met het veiligheidsprofiel uit onderzoeken bij volwassenen en adolescenten met atopische dermatitis.
Kinderen van 6 maanden tot en met 5 jaar oud
De veiligheid van dupilumab met gelijktijdig TCS werd beoordeeld in een onderzoek bij 161 patiënten van 6 maanden tot en met 5 jaar oud met matige tot ernstige atopische dermatitis, waaronder een subgroep van 124 patiënten met ernstige atopische dermatitis (AD-1539). Het veiligheidsprofiel van dupilumab met gelijktijdig TCS bij deze patiënten was tot en met week 16 vergelijkbaar met het veiligheidsprofiel uit onderzoeken bij volwassenen en pediatrische patiënten van 6 tot en met 17 jaar oud met atopische dermatitis.
Atopische hand- en voetdermatitis
De veiligheid van dupilumab werd beoordeeld bij 27 patiënten van 12 tot en met 17 jaar met matige tot ernstige atopische hand- en voetdermatitis (AD-1924). Het veiligheidsprofiel van dupilumab bij deze patiënten tot en met week 16 kwam overeen met het veiligheidsprofiel uit studies bij volwassen en pediatrische patiënten van 6 maanden en ouder met matige tot ernstige AD.
Astma
Adolescenten (12 tot en met 17 jaar oud)
In totaal werden 107 adolescenten van 12 tot en met 17 jaar met astma geïncludeerd in het 52 weken durende QUEST-onderzoek. Het waargenomen veiligheidsprofiel was vergelijkbaar met wat werd gezien bij volwassenen.
De veiligheid op lange termijn van dupilumab werd beoordeeld bij 89 adolescente patiënten die werden geïncludeerd in een open-label uitbreidingsonderzoek naar matig tot ernstig astma (TRAVERSE). In dit onderzoek werden patiënten gevolgd gedurende maximaal 96 weken. Het veiligheidsprofiel van dupilumab in TRAVERSE was consistent met het veiligheidsprofiel dat werd waargenomen in centrale astmaonderzoeken gedurende een behandeling van 52 weken.
Kinderen van 6 tot en met 11 jaar oud
Bij kinderen van 6 tot en met 11 jaar met matig tot ernstig astma (VOYAGE) werd de extra bijwerking enterobiasis gemeld bij 1,8% (5 patiënten) in de dupilumabgroepen en bij niemand in de placebogroep. Alle gevallen van enterobiasis waren licht tot matig en patiënten herstelden met anthelmintische behandeling, zonder stopzetting van de behandeling met dupilumab.
Bij kinderen van 6 tot en met 11 jaar met matig tot ernstig astma werd eosinofilie (≥ 3000 cellen/mcl eosinofielen in het bloed of door de onderzoeker als bijwerking beschouwd) gemeld bij 6,6% in de dupilumabgroepen en bij 0,7% in de placebogroep. De meeste gevallen van eosinofilie waren licht tot matig en gingen niet gepaard met klinische symptomen. Deze gevallen waren van voorbijgaande aard, namen in de loop van de tijd af en leidden niet tot stopzetting van de behandeling met dupilumab.
De veiligheid op lange termijn van dupilumab werd beoordeeld in een open-label uitbreidingsonderzoek (EXCURSION) bij kinderen van 6 tot en met 11 jaar oud met matig tot ernstig astma die eerder hadden deelgenomen aan VOYAGE. Van de 365 patiënten die in EXCURSION werden opgenomen, hadden 350 patiënten 52 weken behandeling afgerond en 228 patiënten hadden een cumulatieve behandelingsduur van 104 weken afgerond (VOYAGE en EXCURSION). Het veiligheidsprofiel op lange termijn van dupilumab in EXCURSION was consistent met het veiligheidsprofiel dat werd waargenomen in centrale astmaonderzoeken gedurende een behandeling van 52 weken.
EoE
Adolescenten (12 tot en met 17 jaar)
In totaal werden 99 adolescenten van 12 tot en met 17 jaar met EoE geïncludeerd in de TREET-onderzoeken (deel A en B). Het waargenomen veiligheidsprofiel was vergelijkbaar met wat werd gezien bij volwassenen.
Kinderen van 1 tot en met 11 jaar
De veiligheid van dupilumab werd beoordeeld in een studie met 101 kinderen van 1 tot en met 11 jaar met EoE (EoE KIDS deel A). Het veiligheidsprofiel van dupilumab bij deze patiënten tot en met week 16 was vergelijkbaar met het veiligheidsprofiel dat werd waargenomen bij volwassen en adolescente patiënten van 12 tot 17 jaar met EoE.
In totaal kregen 98 patiënten die deel A voltooiden de optie om deel te nemen aan een 36 weken durende actieve verlengingsperiode van de behandeling (EoE-KIDS deel B). Het veiligheidsprofiel van dupilumab tot en met week 52 was vergelijkbaar met het veiligheidsprofiel dat werd waargenomen op week 16.
Veiligheid op lange termijn
Atopische dermatitis
Het veiligheidsprofiel van dupilumab + TCS (CHRONOS) bij volwassen patiënten met atopische dermatitis tot en met Week 52 was consistent met het veiligheidsprofiel dat werd waargenomen in Week 16. De veiligheid van dupilumab op lange termijn werd beoordeeld in een open-label uitbreidingsonderzoek bij patiënten van 6 maanden tot en met 17 jaar oud met matige tot ernstige atopische dermatitis (AD‐1434). Het veiligheidsprofiel van dupilumab bij patiënten gevolgd tot en met Week 52 was vergelijkbaar met het veiligheidsprofiel dat werd waargenomen in Week 16 in de onderzoeken AD-1526, AD-1652 en AD-1539. Het veiligheidsprofiel op lange termijn van dupilumab dat werd waargenomen bij kinderen en adolescenten was consistent met wat werd gezien bij volwassenen met atopische dermatitis.
In een multicentrische, open-label fase 3-uitbreidingsonderzoek (OLE) (AD-1225) werd de langetermijnveiligheid van herhaalde doses dupilumab beoordeeld bij 2.677 volwassenen met matige tot ernstige atopische dermatitis (AD) blootgesteld aan toediening van 300 mg per Week (99,7%), waaronder 179 die minstens 260 weken van het onderzoek hadden afgerond. Het langetermijnveiligheidsprofiel dat in dit onderzoek tot 5 jaar is waargenomen, kwam over het algemeen overeen met het veiligheidsprofiel van dupilumab dat waargenomen is in gecontroleerde onderzoeken.
Astma
Het veiligheidsprofiel van dupilumab in het 96 weken durende langetermijnveiligheidsonderzoek (TRAVERSE) was consistent met het veiligheidsprofiel dat werd waargenomen in beslissende astmaonderzoeken gedurende een behandeling van maximaal 52 weken.
Het veiligheidsprofiel van dupilumab bij kinderen van 6 tot en met 11 jaar oud die hadden deelgenomen aan het langetermijnveiligheidsonderzoek van 52 weken (EXCURSION) was consistent met het veiligheidsprofiel dat werd waargenomen in centrale astmaonderzoeken gedurende een behandeling van 52 weken.
CRSwNP
Het veiligheidsprofiel van dupilumab bij volwassenen met CRSwNP tot en met Week 52 was consistent met het veiligheidsprofiel dat werd waargenomen in Week 24.
Eosinofiele oesofagitis
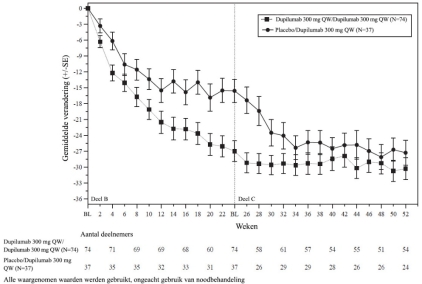
Het veiligheidsprofiel van dupilumab tot en met week 52 bij volwassen en adolescente patiënten van 12 jaar en ouder (TREET deel C) en bij kinderen van 1 tot en met 11 jaar (EoE KIDS deel B) was over het algemeen consistent met het veiligheidsprofiel dat werd waargenomen in week 24 in TREET deel A en B en op week 16 in EoE KIDS deel A.
Melding van vermoedelijke bijwerkingen
Het is belangrijk om na toelating van het geneesmiddel vermoedelijke bijwerkingen te melden. Op deze wijze kan de verhouding tussen voordelen en risico's van het geneesmiddel voortdurend worden gevolgd. Beroepsbeoefenaren in de gezondheidszorg wordt verzocht alle vermoedelijke bijwerkingen te melden via:
België: Federaal Agentschap voor Geneesmiddelen en Gezondheidsproducten: www.fagg.be – Afdeling Vigilantie: Website: www.eenbijwerkingmelden.be – E-mail: adr@fagg-afmps.be
Nederland: Nederlands Bijwerkingen Centrum Lareb – Website: www.lareb.nl
7. HOUDER VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN
Sanofi Winthrop Industrie
82 avenue Raspail
94250 Gentilly
Frankrijk
8. NUMMERS VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN
EU/1/17/1229/005
EU/1/17/1229/006
EU/1/17/1229/008
EU/1/17/1229/017
EU/1/17/1229/018
EU/1/17/1229/020
EU/1/17/1229/026
EU/1/17/1229/027
EU/1/17/1229/028
10. DATUM VAN HERZIENING VAN DE TEKST
01/2025
Gedetailleerde informatie over dit geneesmiddel is beschikbaar op de website van het Europees Geneesmiddelenbureau http://www.ema.europa.eu
PRIJZEN
| CNK code | Verpakking | ATC5 code | Prijs | Af-fabriek prijs | Voorschriftplichtig | Remgeld reguliere tegemoetkoming | Remgeld verhoogde tegemoetkoming |
|---|---|---|---|---|---|---|---|
| 3631108 | DUPIXENT 300MG OPL INJ VOORGEV.SPUIT 2X3 150MG/ML | D11AH05 | € 3505,3 | - | Ja | € 12,5 | € 8,3 |
| 3641941 | DUPIXENT 300MG OPL INJ VOORGEV.SPUIT 1X2 150MG/ML | D11AH05 | € 1175,67 | - | Ja | € 12,5 | € 8,3 |
| 4347811 | DUPIXENT 300MG OPL INJ VOORGEV.PEN 2X3 150MG/ML | € 3505,3 | - | Ja | € 12,5 | € 8,3 | |
| 4347829 | DUPIXENT 300MG OPL INJ VOORGEV.PEN 1X2 150MG/ML | € 1175,67 | - | Ja | € 12,5 | € 8,3 |